فرایند انعقاد و لخته سازی یکی از فرایندهای بسیار پر کاربرد در تصفیه آب و فاضلاب می باشد. فرایند انعقاد و لخته سازی با هدف جداسازی ذرات معلق نامحلول با استفاده از مواد منعقد کننده و لخته ساز انجام می شود. شرکت مهندسی فران طراحی و مجری واحدهای زلال سازی در تصفیه آب و فاضلاب با فرایند انعقاد و لخته سازی است.
*
منابع طبیعی آب خام(چاه، رودخانه و آب دریا) حاوی مقادیری از مواد معلق هستند. ماهیت این مواد معلق می تواند معدنی، آلی و یا بیولوژیک باشد. بازه توزیع اندازه ذرات در نمونه آب بسیار گسترده است و می تواند در محدوده کمتر از 1 میکرون تا چند سانتی متر باشد. هرچه سایز این ذرات کوچکتر باشد، فرایند حذف آن پیچیده تر خواهد بود. شایان ذکر است که آب آشامیدنی سالم فاقد ذرات معلق قابل رویت است.
*
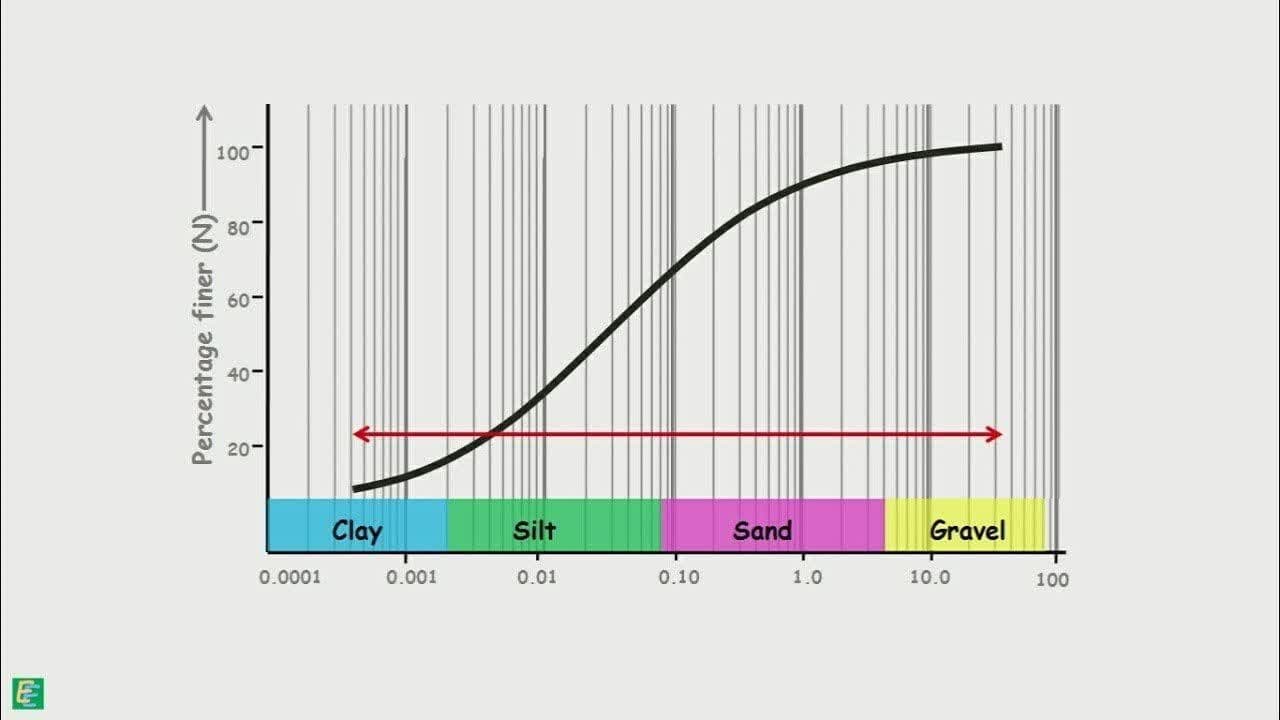
یکی از آزمایش های مهم درخصوص تعیین سایز ذرات معلق، آنالیز توزیع اندازه ذرات(Particle size Distribution.PSD) است. نتیجه این آنالیز منحنی شبیه به منحنی ذیل است.
*
ذرات معلق با ابعاد در حدود سانتی متر را می توان توسط آشغال گیر (Bar Screen) در ورودی به تصفیه خانه ها جداسازی نمود. این تجهیزات در دو نوع دستی و اتوماتیک وجود دارند که نمونه های آن را در شکل ذیل می توان دید.
*
در آب شیرین کن های دریایی در بخش برداشت آب دریا از نوع برداشت سطحی (Open Seawater Intake) معمولاً از تجهیزاتی توری شکل و متحرک (Traveling Band Screen)، با امکاناتی نظیر نازل های شستشو و نیز نازل های توزیع هوای فشرده جهت جداسازی ذرات معلق چسبیده به توری استفاده می شود. معمولاً سایز توری های مورداستفاده در این تجهیزات 2000-1000 میکرون است. در برخی مدل ها نیز این تجهیزات به صورت مرحله ای طراحی می شوند تا در ابتدا ذرات درشت تر و سپس ذرات ریز تر جداسازی شوند.
سازه های دریایی جداسازی ذرات معلق علاوه بر اینکه می بایست از متریال مقاوم در برابر خوردگی ساخته شوند، لازم است با تمهیداتی جهت جلوگیری از آسیبرسانی به اکوسیستم دریایی و ورود جانداران آبزی مجهز شوند. یکی از روش های جلوگیری از ورود ماهی و جانداران آبزی به سازه های برداشت آب دریا استفاده از آنتن های امواج اولتراسونیک جهت فراری دادن آن هاست. ذرات معلق تا سایز 100 میکرون معمولاً توسط فیلترهای فیزیکی که می تواند همراه با تجهیزات شستشوی اتوماتیک باشد از آب حذف می شوند.
*
مکانیسم فرایند انعقاد(Coagulation)
فرایند انعقاد و لخته سازی در واقع تلاشی در جهت ناپایدارسازی و ایجاد برخورد لازم بین ذرات جهت به هم پیوستن آن ها و تشکیل لخته های سنگین تر قابل ته نشینی است.
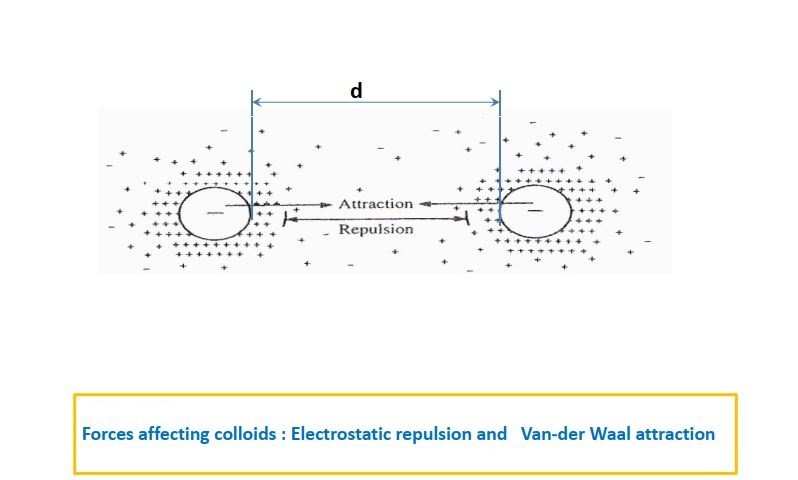
اغلب ذرات کلوئیدی به دلیل جذب سطحی آنیون های آب بار منفی دارند. دافعه الکترواستاتیکی حاصل از این بارهای همنام منجر به عدم ته نشینی آن ها در آب می شود. درون آب لایه ثابتی از یون های مثبت این کلوئیدها با بار منفی را احاطه میکند که این احاطه شدن نیز ناشی از جاذبه الکترواستاتیکی است. این لایه، لایه ثابت (Fixed layer) یا لایه سخت(Stern layer) نامیده می شود.
متعاقب آن، لایه دیگری نیز موسوم به لایه نفوذ (Diffuse layer) ولی با غلظت کمتر (بار کمتر)، لایه ثابت را احاطه می نماید. بر هم کنش این دو لایه با یکدیگر به “تئوری لایه مضاعف” موسوم شده است. سطح بین این دو لایه فوق، سطح تنش (Shear Surface) نامیده می شود. هنگامی که ذره کلوئیدی به حرکت در می آید، بار مثبت چسبیده به ذره کلوئیدی در لایه ثابت به اندازه ای نیست که بتواند بار منفی ذره کلوئیدی را خنثی کند.
پتانسیل الکتریکی در سطح تنش (Shear Surface)، پتانسیل زتا نامیده می شود که معیاری از میزان نیروی دافعه بین ذرات کلوئیدی با بار هم نام است. در فرایندهای مدرن و امروزی انعقاد و لخته سازی، پایش دقیق این پارامتر جهت بهینه سازی فرایند میسر شده است.
فرایند انعقاد (Coagulation) ناپایدارسازی شیمیایی ذرات کلوئیدی است. ذرات کلوئیدی همانطور که در بالا اشاره شد، به دلیل دافعه الکترواستاتیکی نسبت به یکدیگر، پایداری داشته و نسبت به ته نشینی مقاومت می کنند. فرایند خنثی سازی این دافعه الکترواستاتیکی، اصطلاحا ناپایدار ساز(Destabilization) یا انعقاد نامیده می شود.
انعقاد شیمیایی با افزودن یک ماده شیمیایی منعقد کننده (Coagulation) با بار مخالف جهت خنثی سازی دافعه الکترواستاتیکی ذرات کلوئیدی است که شرایط را برای نزدیک شدن این ذرات به یکدیگر و به هم پیوستگی آن ها فراهم می کند.
پس از طی این مرحله، جهت تراکم سازی بیشتر ذرات کلوئیدی به یکدیگر و تشکیل لخته های بزرگتر (Agglomeration) نیاز به ایجاد برخورد بیشتر ذرات با یکدیگر به وسیله فرایند اختلاط است. فرایند اختلاط در این مرحله نباید شدید باشد تا منجر به شکستن و پراکندگی مجدد ذرات لخته شده شود.
تشکیل لخته از ذرات ریز کلوئیدی مشروط بر ناپایدار نمودن ذرات و تجرک ذرات می باشد.
*
ناپایدار نمودن ذرات معلق
ناپایدار نمودن ذرات جهت پیوستگی آن ها به معنای ایجاد تمایل در ذرات به جمع شدن و چسبندگی آن ها با یکدیگر است. نیروی دافعه الکترواستاتیکی بین ذرات کلوییدی با بار همنام نسبت معکوس با فاصله آنها به توان 2 دارد:
از سوی دیگر جاذبه بین ذرات ناشی از نیروی واندروالسی است که به وابستگی قابل توجهی به فاصله بین دو ذره دارد:
دامنه نفوذ پتانسیل الکتریکی دافعه تحت تأثیر تعداد یون های محلول در آب و ظرفیت آن ها شدیداً قابل تغییر است به گونه ای که اگر یک الکترولیت (رسانای) قوی به محلول اضافه شود، این دامنه نفوذ به شدت کاهش می یابد.
از مجموع گزاره های فوق می توان چنین نتیجه گرفت که ناپایداری یک ذره معلق در آب، بدین معناست که برآیند نیروهای واندروالسی (جاذبه) و نیروهای دافعه الکترواستاتیکی (دافعه) موثر به ذره به گونه ای باشد که امکان جاذبه و چسبندگی ذرات با هم فراهم شود.
*
تحرک ذرات معلق
تحرک ذرات از این نظر حایز اهمیت است که شدت تشکیل لخته و چسبندگی ذرات معلق به یکدیگر وابسته به ایجاد شرایطی جهت برخورد بهینه ذرات با یکدیگر است. برخورد ذرات معلق با یکدیگر در یک سیال به دو صورت امکان پذیر است:
*
الف) برخورد طبیعی: برخورد ناشی از انرژی جنبشی ذرات معلق میکروسکوپی در محیط یک سیال مایع یا گازی است. به این حرکت تصادفی ذرات با یکدیگر حرکت براونی (Brownian Motion) نیز می گویند. در مشاهدات میکروسکوپی ذرات به گونه ای حرکت می کنند که گویی از جانب مایع بر آن ها ضربه وارد می آید. مولکولهای سیال به طور دایم به اطراف حرکت می کنند و به ذرات معلق ضربه وارد می کنند و باعث حرکت آن ها میشوند. هرچه دمای مایع بالاتر باشد ذرات با سرعت بیشتری ارتعاش می کنند.
نیروی وارده از سمت مولکول های مایع به اندازه ای ناچیز است که تنها در خصوص ذرات با سایز کمتر از 1 میکرون منجر به ایجاد حرکت (ارتعاش) می شود.
سرعت تغییر در تعداد (غلظت) ذرات (به دلیل برخورد ذرات و چسبندگی آن ها به یکدیگر) در برخورد طبیعی براونی مطابق رابطه ذیل است:
N: غلظت ذرات در سوسپانسیون
t: زمان
α: راندمان برخورد، کسری از کل تعداد برخوردهای بین ذرات که منجر به چسبندگی آن ها و تشکیل لخته درشت تر می شود: (عددی بین صفر و یک)
k: ثابت بولتزمان
T: درجه حرارت به کلوین
µ: ویسکوزیته مایع
با انتگرالگیری از طرفین معادله فوق خواهیم داشت:
در دمای 20 درجه سانتی گراد، مقدار برابر با 15-10×5/4 لیتر بر ثانیه است. اگر سوسپانسیونی از خاک رس در آب به غلظت 109 ذره در لیتر داشته باشیم و فرض کنیم تمامی برخوردها منجر به چسبندگی ذرات به یکدیگر شوند (1=α)، با استناد به رابطه فوق می توان چنین نتیجه گرفت که حداقل 2 روز طول خواهد کشید تا تعداد ذرات موجود در سوسپانسیون به نصف کاهش یابد، لذا اکتفا به این نوع حرکت در مقیاس واقعی طراحی، منطقی نیست.
از معادله اخیر همچنین میتوان نتایج ذیل را استنباط نمود:
- هرچه دمای سیال بیشتر شود، تعداد برخوردها و در نتیجه سرعت تغییر در تعداد ذرات افزایش خواهد یافت.
- هرچه ویسکوزیته سیال بیشتر باشد، حرکت براونی ضعیف تر خواهد شد.
- هرچه غلظت اولیه ذرات معلق بیشتر باشد، سرعت تغییر غلظت ذرات به دلیل چسبندگی آنها با یکدیگر نیز بیشتر است. در مثال عددی اخیر اگر غلظت اولیه ذرات به جای 109 ذره بر لیتر، 108 ذره بر لیتر باشد، بیش از 20 روز لازم است تا این غلظت به نصف کاهش یابد!
*
ب) برخورد اختلاطی (Bulk Motion):
در این حالت با استفاده از عاملی خارجی نظیر حرکت توده سیال و یا به کارگیری تجهیزی مانند هم زن مکانیکی، فرکانس برخورد ها افزایش یافته تا در زمان کوتاه تری چسبندگی ذرات با یکدیگر اتفاق بیفتد. در شرایطی که برخورد ذرات با یکدیگر ناشی از حرکت توده سیال باشد، تشکیل ذرات درشت تر (لخته سازی) را اورتوکینتیک (Orthokinetice) مینامند.
سرعت تغییر در تعداد (غلظت) ذرات موجود در سوسپانسیون در حالت اورتوکینتیک طبق رابط ذیل است:
d: قطر ذرات
G: گرادیان سرعت متوسط سیال
از رابطه فوق چنین می توان نتیجه گرفت که در سرعت های یکسان تغییر در غلظت سوسپانسیون، گرادیان سرعت مورد نیاز، وابستگی شدید به قطر ذرات دارد. مثلاً اگر قطر ذره ای 1 میکرون باشد در مقایسه با ذره ای به قطر 0/1 میکرون، لازم است گرادیان سرعت متوسط سیال هزار برابر افزایش یابد تا همان Jok حاصل شود.
گرادیان سرعت متوسط سیال از رابطه ذیل به دست می آید که استنتاج آن با استفاده از معادله دیفرانسیل تنش برشی و پروفایل سرعت سیال از موضوع این نوشتار خارج است:
که در آن:
G: گرادیان سرعت متوسط (sec-1)
P: توان مصرفی جهت اختلاط سیال
V: حجم مایع درون مخزن
µ: ویسکوزیته مطلق سیال
ج) برخورد حاصل از ته نشینی دیفرانسیلی: (Differential Setting)
ذرات با سایز بزرگتر سرعت ته نشینی بیشتری دارند. در حین حرکت این ذرات به سمت کف مخزن ته نشینی، ممکن است برخوردی بین آن ها با ذرات با سایز کمتر که سرعت ته نشینی کمتری دارند اتفاق بیفتد که این برخورد منجر به چسبندگی ذرات ریز تر به ذرات با سایز درشت تر خواهد شد.
*
شیمی فرایند انعقاد
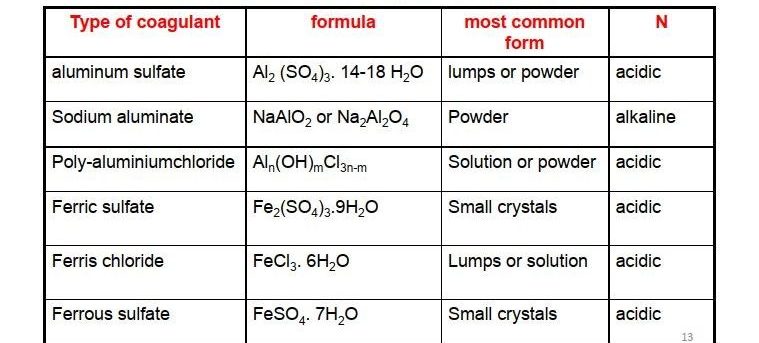
مهم ترین مواد شیمیایی منعقد کننده در جدول زیر گردآوری شده است:
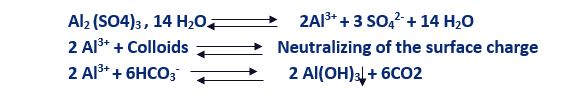
اگر از آلوم جهت فرایند انعقاد استفاده شود، واکنش های ذیل را خواهیم داشت:
همانطور که مشاهده میکنیم، افزودن آلوم منجر به مصرف قلیائیت آب و ایجاد شرایط اسیدی خواهد شد:
در شرایطی که قلیائیت آب کافی نباشد، لازم است با افزودن آب آهک PH افزایش یابد.
*
عوامل موثر بر فرایند انعقاد
بهترین عوامل موثر بر فرایند انعقاد عبارت اند از:
- میزان تزریق ماده منعقد کننده
- PH نمونه
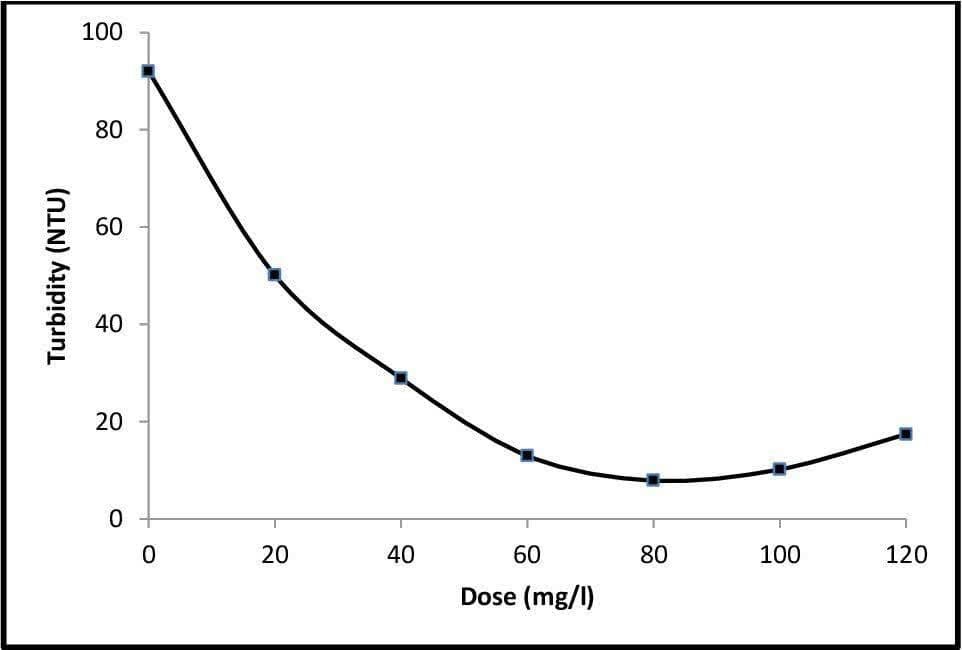
تنظیم و حصول شرایط بهینه دو پارامتر فوق توسط آزمایش جار (Jar test) صورت می گیرد. که نمونه ای از منحنی خروجی این آزمایش در شکل زیر نمایش داده شده است:

*
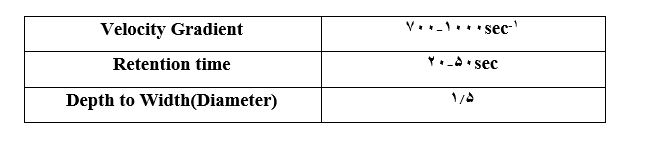
معیارهای طراحی فرایند انعقاد
معیارهای طراحی فرایند لخته سازی (Flocculation)
رابطه محاسبه توان هم زن پارویی (Paddle Mixer)
که در آن:
در خصوص سایر انواع همزن های مکانیکی رابطه محاسبه توان با سرعت طبق معادله ذیل است:
که در آن:
P: توان مورد نیاز به وات
ꝩ: وزن مخصوص
g: شتاب گرانشی
N: سرعت چرخش پروانه (rps)
Da: قطر پروانه (m)
k: ثابت بدون بعد
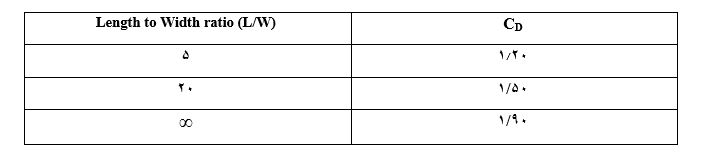
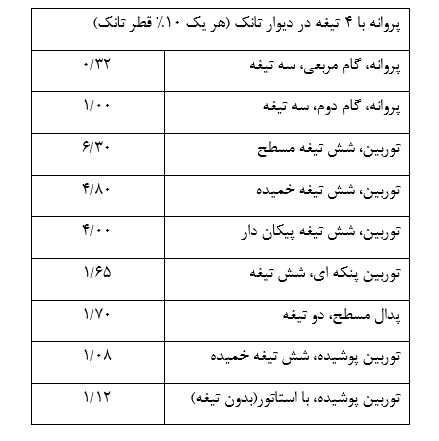
مقدار k به شرایط جریان (آرام و آشفته) بستگی دارد که در جدول زیر آمده است:
*
نکات تکمیلی در فرایند انعقاد
انعقاد و لخته سازی موضوعی بسیار گسترده و پرداختن به کلیه مباحث تئوری آن در قالب این نوشتار امکان پذیر نیست.
لذا به صورت تیتروار به برخی از مهمترین موضوعات کاربردی در این خصوص اشاره می شود:
- هرچه کدورت و قلیائیت آب بیشتر باشد، انعقاد راحت تر انجام می شود. انعقاد در شرایط کدورت و قلیائیت کم بامشکلات فراوانی همراه است که گاهی لازم است تعمدا کدورت آب خام با افزودن مواد معلق مانند خاک رس یا شیر آهک افزایش یابد.
- برای آب های طبیعی که حاوی رنگ هستند، اکسید منیزیم کارایی بسیار خوبی در انعقاد و حذف رنگ دارد. اگر آب به طور طبیعی حاوی منیزیم باشد، می توان با افزودن آهک به آن منیزیم را به فرم هیدروکسید منیزیم که حالت ژلاتینی دارد تبدیل نمود که با محبوس نمودن ذرات معلق در خود کدورت و رنگ را به میزان قابل توجهی کاهش خواهد داد.
- وجود گاز دی اکسیدکربن در آب به طور طبیعی و یا ناشی از افزودن ماده منعقد کننده عاملی مزاحم است چون باعث شناوری مجدد ذرات شده و از ته نشینی آن ها جلوگیری میکند. لذا کنترل PH در فرایند انعقاد ضروری است.
- استفاده از آلوم (سولفات آلومینیوم هیدراته) در آب های فاقد سختی منجر به بروز خوردگی می شود. در این شرایط بهتر است از آلومینات سدیم استفاده شود. این ماده علاوه بر خاصیت منعقد کنندگی، به افزایش قلیائیت آب کمک میکند.
- باقیمانده یون آلومینیوم در خروجی تصفیه خانه های آب شرب، مشکلات بهداشتی قابل توجهی به دنبال دارد. ثابت شده است که این یون ریسک ابتلا به آلزایمر را افزایش می دهد. لذا ضمن پایش دقیق باقیمانده این یون در آب تصفیه شده لازم است از منعقد کننده هایی استفاده شود که محتوای آلومینیوم باقیمانده آن ها در آب، حداقل ممکن باشد.
- از بین منعقد کننده های معدنی، تنها کلرید آهن سه ظرفیتی در آب سرد قدرت منعقدکنندگی دارد.
- در خصوص حذف فسفات از فاضلاب تصفیه شده، استفاده از کلرید آهن سه ظرفیتی بسیار موثر است.
- پس از انجام فرایند انعقاد و لخته سازی، در فاز ته نشینی شرایط باید به گونه ای باشد که رسوب تشکیل شده حداقل حلالیت را داشته باشد. لذا تنظیم PH جهت جلوگیری از انحلال مجدد رسوب، بسیار ضروری است.
*
کمک منعقد کننده ها (Flocculant, Coagulant aid)
برخی از الکترولیت ها که ساختاری زنجیری و باردار دارند، می توانند کارایی فرایند انعقاد و لخته سازی را با تولید لخته هایی سنگین تر و متراکم تر بهبود بخشند.
علی رغم گران بودن این مواد در مقایسه با منعقد کننده های معدنی، به دلیل میزان بسیار کم تزریق آن به آب، به کارگیری آن ها اقتصادی است.
مکانیسم اثر این مواد ایجاد پل بین ذرات لخته شده و اتصال آن ها با یکدیگر است. به کارگیری این مواد که در فرم های غیر یونی، کاتیونی و آنیونی تولید می شوند، می تواند گستره PH بهینه فرایند انعقاد را نیز تغییر داده و باعث بهبود کارایی فرایند شوند. اگر ظرفیت تصفیه خانه و میزان کدورت ورودی کم باشد، بعضا می توان از پلی الکترولیت کاتیونی به تنهایی جهت انعقاد و لخته سازی استفاده نمود.
برای کسب اطلاعات بیتشر بر روی فایل مقاله “فرایند انعقاد و لخته سازی” کلیک کنید.
شرکت مهندسی فران با تکیه بر تجربه بیش از 17 سال تجربه حرفه ای در صنعت تصفیه آب صنعتی و تصفیه فاضلاب صنعتی، واحدهای زلال سازی را با فرایندهای مختلف نظیر فرایند انعقاد و لخته سازی طراحی و اجرا می کند.




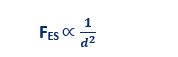
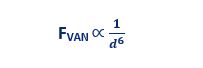
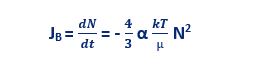
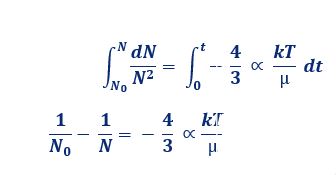
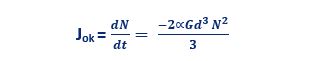
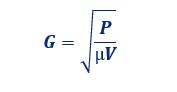

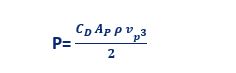

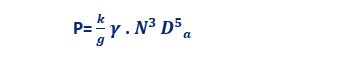
2 پاسخ
سپاس از مطالب کاربردیتون .عالی بود
ممنون از بازخورد شما